硝化と脱窒【窒素循環について】
有機窒素から無機窒素へ【まずはアンモニア(NH3)】
まず無脊椎動物にしろ海水魚にしろ生き物である以上、何らかの餌を食べ、排泄し、いずれは死亡します。つまり、これらを排除しないかぎりはタンク内に餌の食べ残しや排泄物、亡骸などが溜まっていってしまうことになります。ま、これらが何の変化も起こさなければ、放っておいても見栄えが悪くなるだけのことですし、固形物は物理的に取り出してしまえば良いことになります。(←極論すれば、これが物理濾過ですね)しかし、幸か不幸か必ず分解作用が始まり、結果生き物に悪影響を及ぼす物質(無機窒素)への変化していきます。
生き物(餌や排泄物もそうですが)はタンパク質をはじめとする様々な有機窒素化合物から構成されています。この有機窒素は、不溶性有機窒素と水溶性有機窒素に分けることができます。まず、不溶性有機窒素である残り餌や排泄物、死体などは水溶性有機窒素へ分解され、水溶性有機窒素ははアンモニア(NH3)へと変化します。
生物の排泄物である尿素(CO(NH2)2)はウレアーゼと呼ばれる尿素分解酵素によって二酸化炭素(CO2)とアンモニア(NH3)に分解されます。
CO(NH2)2 + H2O → 2NH3 + CO2
アンモニア(NH3)とアンモニウムイオン(NH4+)
このアンモニアはタンク内の生物にとっては猛毒です。アンモニアがタンク内に0.1mg/L以上存在すると簡単に海水魚などの生物は昇天致します。しかしこのアンモニアは非常に不安定な物質で、あまりアンモニアのままで存在していることができず(非常に水に溶けやすい性質なので)、ほとんどは水に溶けて無害なアンモニウムイオン(NH4+)へと変化してしまいます。タンク立ち上げ時にアンモニア試薬で測ったアンモニア値がかなり高いのにパイロットフィッシュなどが死なないのは、ほとんどのアンモニア試薬が総アンモニア量(NH4+とNH3の総量)を測っていて実際のアンモニアは測定値よりかなり低い為です。このアンモニアとアンモニウムの関係を化学式で表すと次のようになります。
NH3 + H2O ←→ NH4+ + OH-
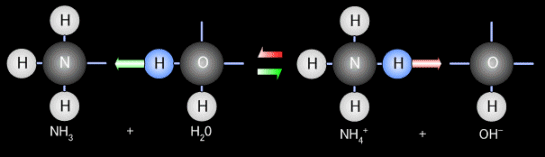
わかりやすくするために概念的なモデル図を書いてみました(あくまでもイメージですのであしからず)。アンモニアがアンモニウムイオン化する場合、アンモニア(NH3)は水(H2O)から水素イオン(H+)を受け取ってアンモニウムイオン(NH4+)へと変化し、水素イオンをとられた水(H2O)は水酸イオン(OH-)へと変化します。逆にアンモニウムイオンからアンモニアへ変化する場合もあり、この場合は前記と逆の事が起きます。しかし、このアンモニウム(NH4+)は温度の上昇やpHの上昇で簡単にアンモニア(NH3)へ戻ってしまいます。アンモニアは同一温度ではpHが高い方が多く存在し、同一pHでは温度が高い方が多く存在します。
22℃ pH7.8 → 2.8%がアンモニア
28℃ pH7.8 → 4.0%がアンモニア
22℃ pH8.4 → 10.2%がアンモニア
つまりタンク内のほとんどが無害なアンモニウム(NH4+)なのですが、温度の上昇やpHの上昇で一気にアンモニアの量が増加する事が考えられます。なので、総アンモニア量は極限まで引き下げるべきです。(通常の立ち上がったタンクであればアンモニアはほとんど検出されないとは思いますが)
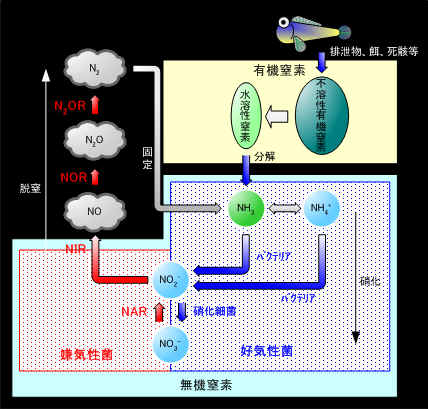
窒素循環
無機化された物質がバクテリアによって硝化と還元を繰り返す事を窒素循環といいます。窒素循環は窒素固定(nitrogen fixation)、硝化(nitrification)、および脱窒(denitrification)により構成されます。窒素固定 N2 → NH4多くの濾過装置は、好気バクテリアによる硝化作用のみを期待し、硝酸は人間の手で排出する方法がとられています。しかし、実際の自然界では硝化した硝酸を窒素に戻す還元(脱窒)が行われています。
硝化 NH4+ → NO2- → NO3-
脱窒 NO3- → NO2- →NO → N2O→N2
【好気バクテリアによる硝化(酸化)】
有機物が分解された結果、生成されたアンモニア(NH3)はアンモニア酸化菌(Nitrosomonas:ニトロソモナス属等)によって亜硝酸イオン(NO2-)を生成します。
NH3 + (3/2)O2 → NO2- + H2O + H+
次に亜硝酸酸化菌(Nitrobacter:ニトロバクター属等)が亜硝酸イオンを呼吸基質として取り込み酸化することによって硝酸イオン(NO3-)を生成します。
NO2- + (1/2)O2 → NO3-
となります。アンモニア酸化菌、亜硝酸酸化菌を総称して硝化菌と呼び、アンモニアから硝酸への変化は
NH3 + 2O2 → NO3-
+ H2O + H+
という化学式で書くことができます。つまりタンク内でアンモニアから硝酸へと生物濾過が働くと、酸素が消費され、水と水素イオンが増加することになります。水素イオンが増加するということはタンクのpHが下がり酸性化していくことになるわけです。
ここまでの反応が好気バクテリアによる生物濾過の過程です。好気バクテリアによる濾過だけだと硝酸が最終物となるので。硝酸は消えることなくタンク内に蓄積されていき、何もしなければpHもどんどん下がってくることになります。好気バクテリアのみに依存する濾過方法では、定期的に水替えを行って硝酸を取り出してやらなければならなくなります。
【嫌気バクテリアによる脱窒(還元)】
嫌気バクテリアたちが好気バクテリアの過程を逆に進むようにして、硝酸を窒素へと変化させていくことを脱窒反応といいます。NO3- → NO2- → NO → N2O → N2
2NO3- + 2H2 → 2NO2- + 2H2O
2NO2- + 3H2 → N2 + 2H2O + 2OH-
硝酸が窒化するまでの式をまとめると、つぎのようになります。
2NO3- + 5H2 → N2 + 4H2O + 2OH-
化学式をみても分かるように、還元が行われると水素が消費され、素酸イオンが生成されるのでpHは上昇してアルカリに傾いていくことにになります。つまり、酸化ー還元の窒素循環が上手くタンク内で実現できれば、水替えを行わなくても硝酸が蓄積されず、なおかつpHも安定した値を保つことができることになります。ただし注意しなければならないのは、プロテインスキーマなどにより、微量元素が削除されたり、サンゴなどがカルシウムやヨウ素、ストロンチウムなどを消費していくので水替えを行わないのであれば、これを補うために添加剤によって不足元素を補充する必要が出てきます。